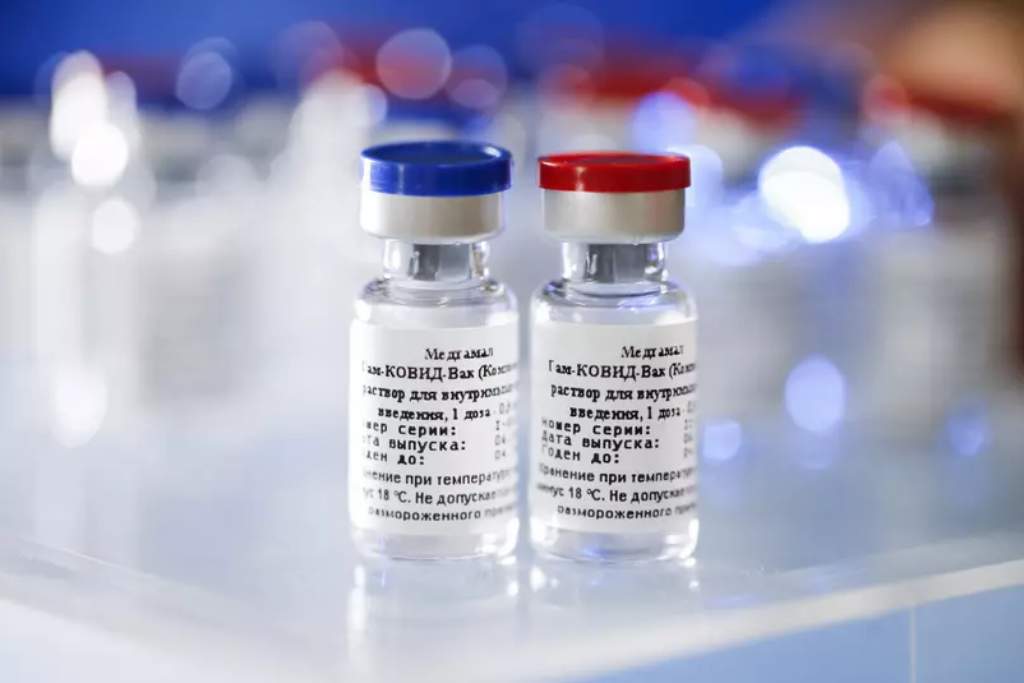
A Agência Nacional de Vigilância Sanitária (Anvisa) realiza, neste domingo (17), em Brasília, reunião extraordinária de sua diretoria colegiada, formada por cinco integrantes, para analisar os pedidos de autorização temporária de uso emergencial de duas vacinas contra a covid-19.
A reunião começa às 10h e tem previsão de cinco horas de duração.

Estão na pauta da Anvisa os processos do imunizante Coronavac, fabricado e desenvolvido pelo Instituto Butantan, em conjunto com a farmacêutica chinesa Sinovac; e o da vacina da Fundação Oswaldo Cruz (Fiocruz), desenvolvida pela Universidade de Oxford, na Inglaterra, em parceria com o laboratório AstraZeneca.
Somados, os pedidos se referem a seis milhões de doses da Coronavac e outros dois milhões de doses da vacina da Astrazeneca/Oxford.
Segundo comunicado da Anvisa, os pedidos serão analisados de forma separada e a decisão de aprovar o uso emergencial ou não será tomada por maioria simples, ou seja, de cinco diretores, três votos a favor ou contra definirão o resultado.
Apresentação
Após a abertura da reunião, três áreas técnicas da Anvisa farão uma apresentação: área de medicamentos, que avalia os estudos clínicos e de eficácia e segurança; a área de certificação de boas práticas de fabricação, que verifica se os locais de fabricação da vacina têm condições adequadas; e a área de monitoramento de eventos adversos, que monitora e investiga depois da vacinação se as pessoas tiveram alguma reação à vacina.
De acordo com o painel da Anvisa que atualiza o andamento dos pedidos, atualizado por volta das 16h deste sábado (16), a Coronavac tinha 62,12% da documentação analisada, restando 37,86%. Já a vacina da AastraZeneca/Oxford, em parceria com a Friocruz, aparecia com 85,12% de análise concluída, restando ainda 14,88% de documentação a ser examinada.
Terminada a apresentação das áreas técnicas, a diretora-relatora dos dois processos, Meiruze Freitas, passará a ler o voto. Em seguida, cada um dos demais diretores vota concordando ou discordando do voto da relatora. São eles: Antonio Barra (diretor-presidente), Cristiane Jourdan, Romison Mota e Alex Campos.
Resultado da votação
Na sequência, o resultado da votação é anunciado pelo diretor-presidente da Anvisa. A decisão passa a valer a partir do momento em que houver comunicação oficial aos laboratórios que fizeram o pedido. O resultado também é publicado no portal da Anvisa e não precisa de publicação no Diário Oficial da União para entrar em vigor.
Na última semana, o presidente Jair Bolsonaro e o ministro da Saúde, Eduardo Pazuello, informaram que a vacinação deve ter início ainda em janeiro, para um público prioritário formado por profissionais de saúde que atuam na linha de frente da pandemia, idosos e indígenas. A data, no entanto, ainda não foi definida, e dependerá da logística prévia de distribuição dos imunizantes para centros de vacinação em todo o país, o que levará alguns dias, além do detalhamento sobre o público-alvo nesta primeira fase.
O governo dispõe, neste momento, de seis milhões de doses da Coronavac, armazenadas no Instituto Butantan, em São Paulo. Outros dois milhões de doses da vacina da AstraZeneca/Oxford, que podem ser importadas da Índia nos próximos dias, terão a entrega atrasada, de acordo com o Ministério das Relações Exteriores.